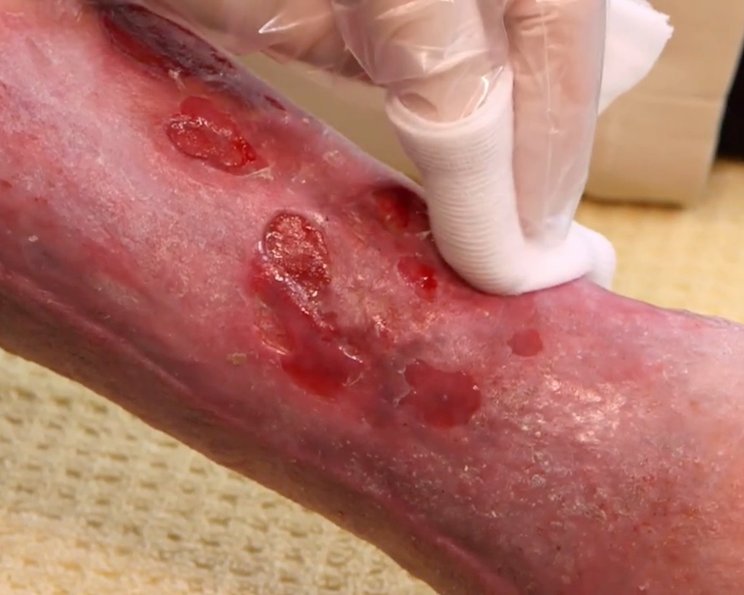
Débridement – Definition, Methoden und Durchführung
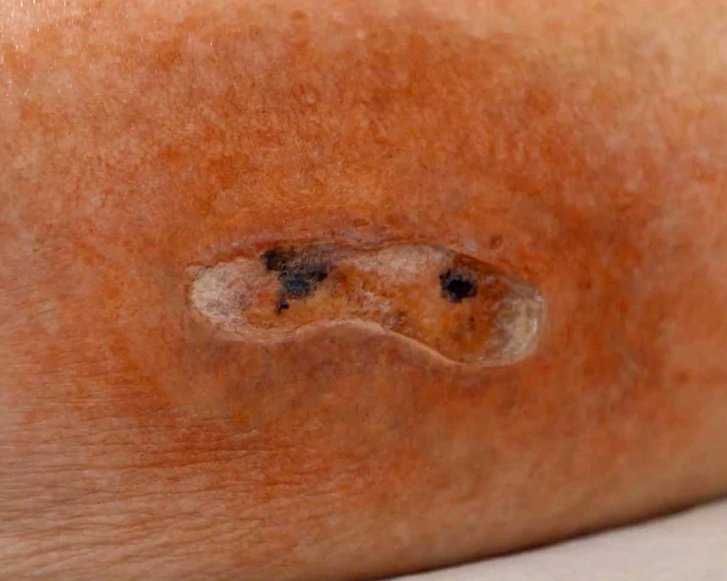
Débridement (zu Deutsch: Wundtoilette) bezeichnet die Entfernung von anhaftendem, abgestorbenem oder kontaminiertem Gewebe aus akuten oder chronischen Wunden. Das Débridement fördert den Prozess der Wundheilung und ermöglicht die Einschätzung von Umfang und Zustand der Wunde.
Indem Störfaktoren wie nekrotische oder fibrinöse Beläge beseitigt werden, lässt sich der Wundgrund adäquat beurteilen und ein mögliches Risiko für Wundinfektionen erkennen. Ein Débridement reduziert die Infektionsgefahr, mindert Gerüche und Exsudatbildung, stimuliert Wundränder und die Epithelisierung und trägt somit zu einer besseren Lebensqualität der Patienten bei.
Débridement: Welche Arten gibt es?
Es gibt in der Wundbehandlung verschiedene Arten des Débridements.
Die Wahl des am besten geeigneten Verfahrens hängt zum einen von der Wundsituation (Wundart, der Lokalisation, der Wundtiefe und Beschaffenheit der Wunde), zum anderen von individuellen Faktoren (z.B. Räumlichkeiten, Ausstattung, Zeit, Kosten) und Kenntnissen/Erfahrungen ab. Zum anderen sind die Gesamtsituation des Patienten sowie mögliche Präferenzen und Ängste bei der Wahl der Débridement-Methode zu berücksichtigen.
Debridement: Fortbildung mit DRACO Wunde+
| Art | Wichtigste Merkmale | Produkte / Instrumente |
|---|---|---|
Autolytisches Débridement |
| Hydrogele, Gelkompressen, Alginate, Hydrofasern, Hydrokolloide oder Nasstherapeutika |
Biochirurgisches Débridement (Larven-, früher Madentherapie) |
| BioBag®, Freiläufer Fliegenlarven |
Chirurgisches Débridement |
| Skalpell, Schere, chirurgische Pinzette, scharfe Löffel, Ringkürette |
Enzymatisches/proteolytisches Débridement |
| Gele oder Salben mit proteolytischen Enzymen (z.B. Kollagenase) |
Mechanisches Débridement |
| sterile Baumwollkompressen / Gazekompressen, Monofilamentfaser-Pads (Mikrofaserpads), Wundreinigungstuch |
Osmotisches Débridement |
| Honigpräparate, Dextranomer-, Cadexomerpräparate |
technisches Débridement |
| Ultraschallgerät, Hydrochirurgie, Laser |
Alle Débridementarten – mit Ausnahme des chirurgischen Débridements – können je nach Ausbildungsgrad an nichtärztliches Personal, zum Beispiel MFA oder Pflegekräfte, delegiert werden. Der Arzt ist hierbei verpflichtet, sich im Vorfeld von der Kompetenz des nichtärztlichen Personals zu überzeugen.
Invasive Eingriffe hingegen sind nur von qualifiziertem ärztlichem Personal vorzunehmen.
Das Durchführen eines Débridements wird in der Medizin "débridieren" genannt und bezeichnet - unabhängig von der eingesetzten Débridement-Methode - das Entfernen von Wundbelägen und abgestorbenem Gewebe aus einer Wunde.
Video: Débridement, Wundreinigung
Bei Start des Videos werden Informationen an YouTube/Google übermittelt. Mehr hierzu unter: Google Datenschutzerklärung.
Unter einem Débridement versteht man das Entfernen von Nekrosen und Belägen. Es gibt verschiedene Débridementarten, die in diesem Video erläutert werden.
Die Wundreinigung ist definiert als das Entfernen von Verschmutzungen und Fremdkörpern durch mechanisches Ausspülen bzw. Auswischen der Wunde.
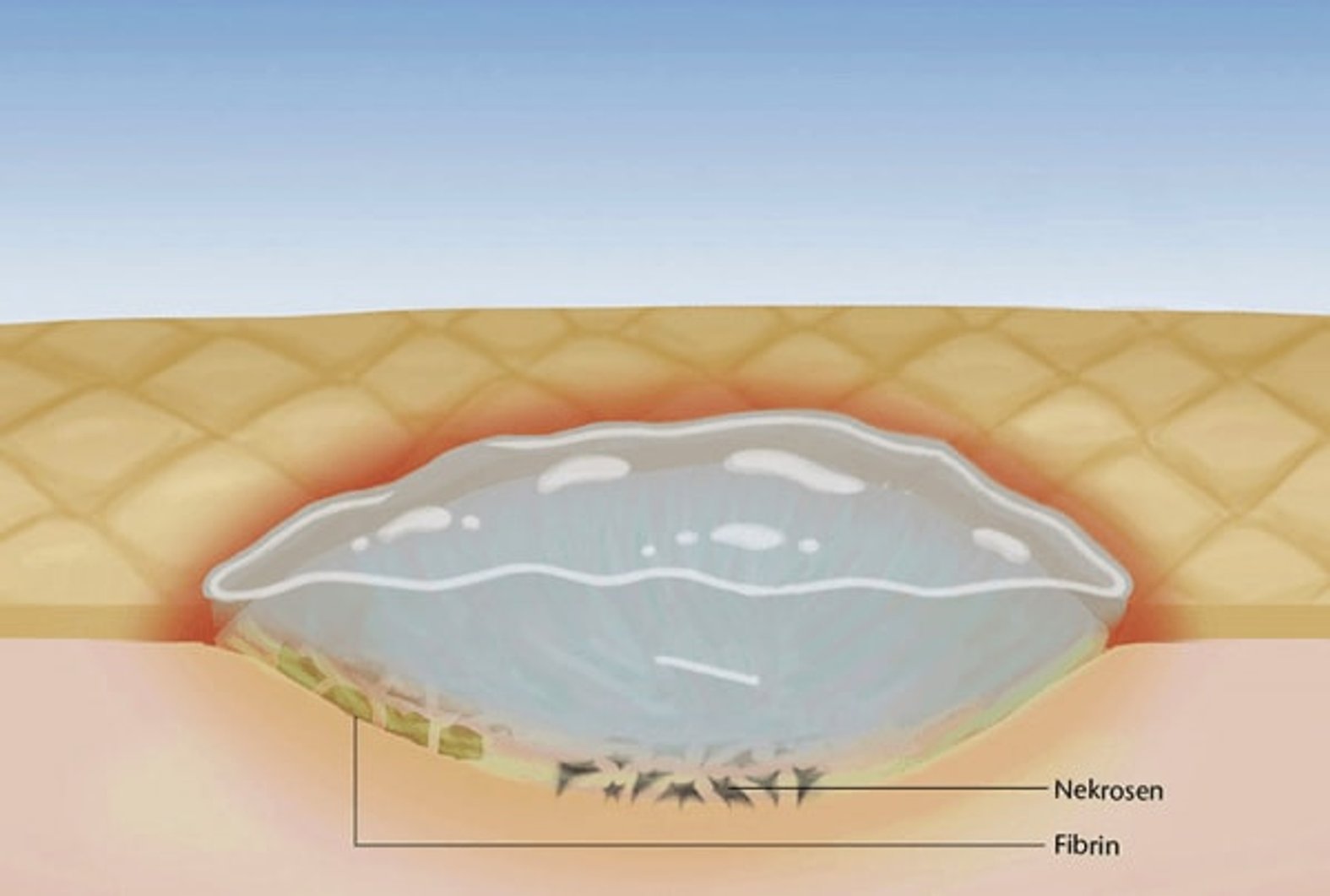
Débridement beschreibt die tiefgreifende Entfernung von anhaftendem, abgestorbenem oder kontaminiertem Gewebe aus Wunden. Beläge oder Nekrosen auf chronischen Wunden können den Prozess der Wundheilung behindern. Vorrangiges Ziel des Débridements ist es, diese Beläge wie z. B. Nekrosen, Fibrin, Schorf, Krusten und Detritus aus der Wunde zu entfernen und günstige Bedingungen für den Heilungsprozess zu schaffen.
Autolytisches Débridement
Beim autolytischen Débridement werden nekrotische und fibrinöse Wundbeläge mithilfe von feuchtigkeitsspendenden Gelen und Wundauflagen aufgeweicht und entfernt.
Zudem wird Flüssigkeit aus mäßig bis stark nässenden Wunden absorbiert. Es ist eine schonende und nahezu schmerzfreie, aber auch sehr zeitintensive Form des Débridements in der Wundversorgung. Im Klinikalltag wird diese Methode deswegen nicht sehr häufig angewendet, wohingegen sie in der ambulanten Pflege häufiger zum Einsatz kommt.
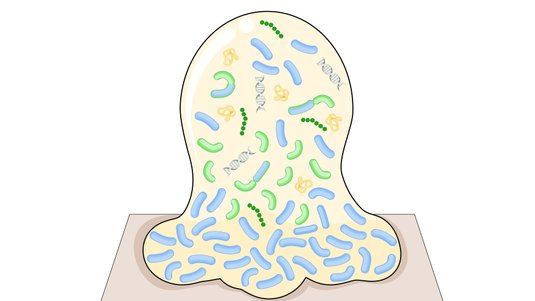
Das autolytische Débridement macht sich die physikalische Wirkung von Flüssigkeit auf Beläge zunutze: Hydrogele zum Beispiel weichen durch ihre Feuchtigkeit Nekrosen und Fibrin auf. Es unterstützt den Autolyseprozess, d.h. die Freisetzung körpereigener proteolytischer Enzyme und Aktivierung von Immunzellen, die das abgestorbene Gewebe aufweichen und Beläge vom Wundgrund lösen und zersetzen. Danach sind diese leichter aus der Wunde zu spülen bzw. zu entfernen.
Durchführung
Das autolytische Débridement ist mithilfe verschiedener Produkte umsetzbar:
Hydrogele: Hydrogele aus der Tube bestehen bis zu 95% aus Wasser. Bei infizierten Wunden sind Wundgele mit antiseptischen Zusätzen indiziert. Sie werden direkt auf den Wundbelag aufgetragen und mit einem Sekundärverband abgedeckt, der das feuchte Wundmilieu erhält. Je nach Exsudatmenge kann es sich dabei z.B. um sterile semipermeable Transparentfolie oder um feinporige Polyurethanschaumverbände handeln. Das Entfernen der aufgeweichten Wundbeläge erfolgt durch die Pflegekraft im Rahmen des Verbandwechsels.
Neben der nahezu schmerzfreien Anwendung besteht ein wesentlicher Vorteil von Wundgelen in der guten Applizierbarkeit auch an schwierigen Körperstellen, z. B. im Fersenbereich. Bei ausgedehnten Fibrinbelägen oder Nekrosen reicht ein autolytisches Débridement jedoch meist nicht aus – in diesem Fall sollte zusätzlich z.B. ein chirurgisches Débridement durchgeführt werden.
Achtung: Trockene Nekrosen sollten trocken – also nicht mit Hydrogelen – behandelt werden, weil sonst die Gefahr einer Infektion besteht. Auch bei stark nässenden oder blutenden Wunden sollte von der Anwendung von Wundgelen abgesehen werden.
Alginate und Hydrofaser: Alternativ zu Hydrogelen können saugfähige Alginate und Hydrofasern bei größeren Exsudatmengen eingesetzt werden. Genau wie Hydrogele benötigen beide Wundauflagen einen Sekundärverband. Zudem sind die Anwendungshinweise zum jeweiligen Produkt zu beachten. Alginate wie DracoAlgin haben eine leicht blutstillende Wirkung, dürfen aber beispielsweise im Gegensatz zu Hydrofasern wie DracoHydrofaser nicht über den Wundrand überlappend aufgelegt werden, da es zur Mazeration des Wundrands und der Wundumgebung führen kann.
Hydrokolloidverbände: Auch hydrokolloide Wundauflagen finden im Rahmen des autolytischen Débridements bei sehr dünnen nekrotischen oder fibrinösen Wundbelägen, die eine hohe Feuchtigkeit aufweisen, Anwendung. Hydrokolloidverbände sind bei infizierten Wunden kontraindiziert.
Achtung: Bei Patienten mit Diabetes mellitus oder infizierten Wunden sollten Hydrokolloidverbände nur mit besonderer Vorsicht und mit ärztlicher Absprache zum Einsatz kommen. Sie schaffen hervorragende Bedingungen für Bakterien, sich schnell zu vermehren und können eine Sepsis herbeiführen. (Quelle: Strohal, Dissemond, et al. 2013)
Biochirurgisches Débridement (Larventherapie)
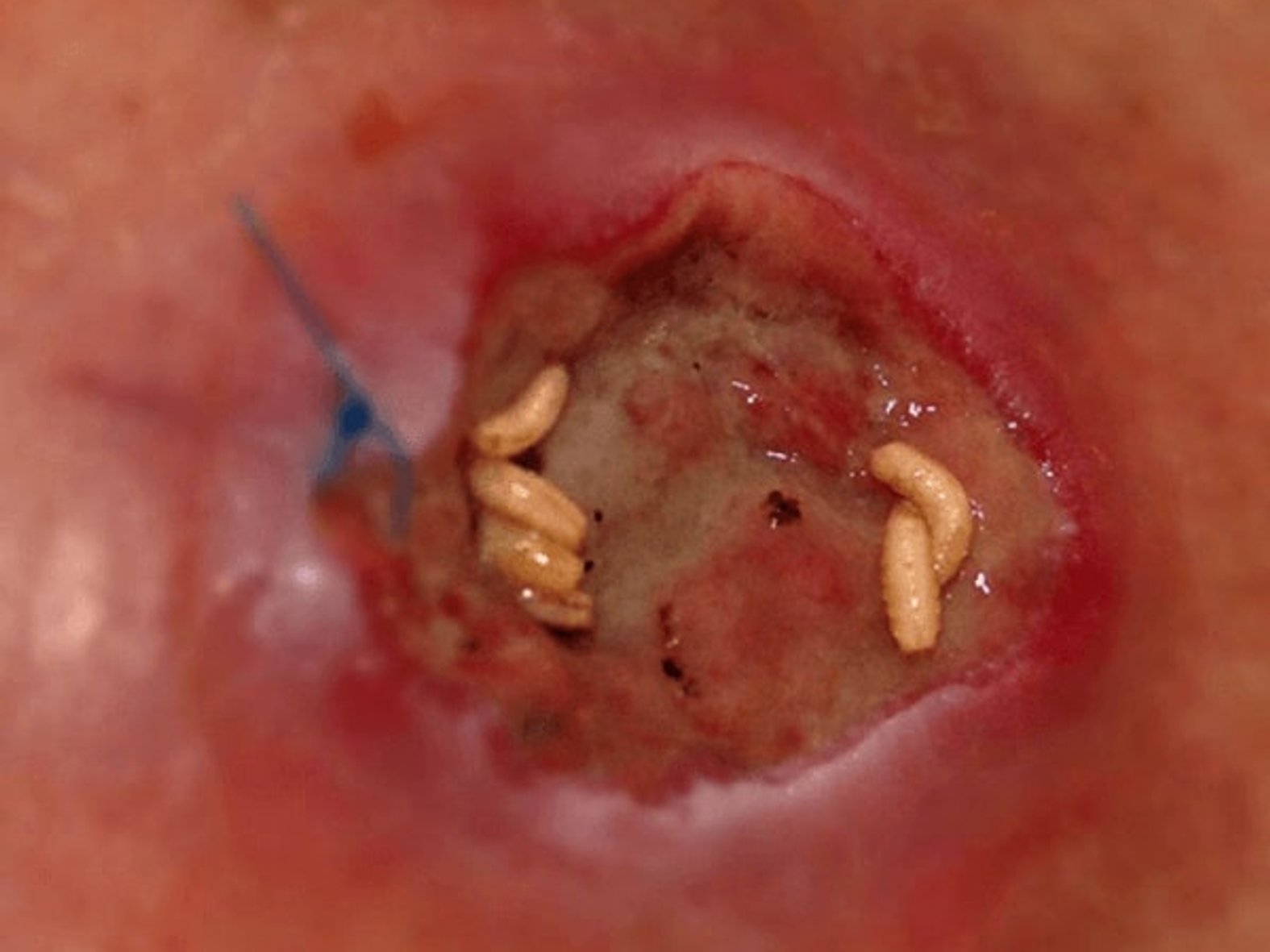
Beim biochirurgischen Débridement (auch Larventherapie, früher Madentherapie genannt) werden steril gezüchtete Larven der Fliege Lucilia sericata eingesetzt.
Mithilfe ihres Speichels, der proteolytische Enzyme enthält, tragen die Fliegenlarven vor allem hartnäckige Nekrosen durch Verflüssigung ab und nehmen den entstehenden Brei als Nahrung wieder auf. Bei Versuchen in der Petrischale konnte zudem nachgewiesen werden, dass diese Larven auf einem Keimrasen eine bakterienfreie Spur hinterlassen. Die Methode kommt vor allem dann zum Einsatz, wenn das nötige Untergewebe für ein chirurgisches Débridement fehlt.
Bei Start des Videos werden Informationen an YouTube/Google übermittelt. Mehr hierzu unter: Google Datenschutzerklärung.
Durchführung
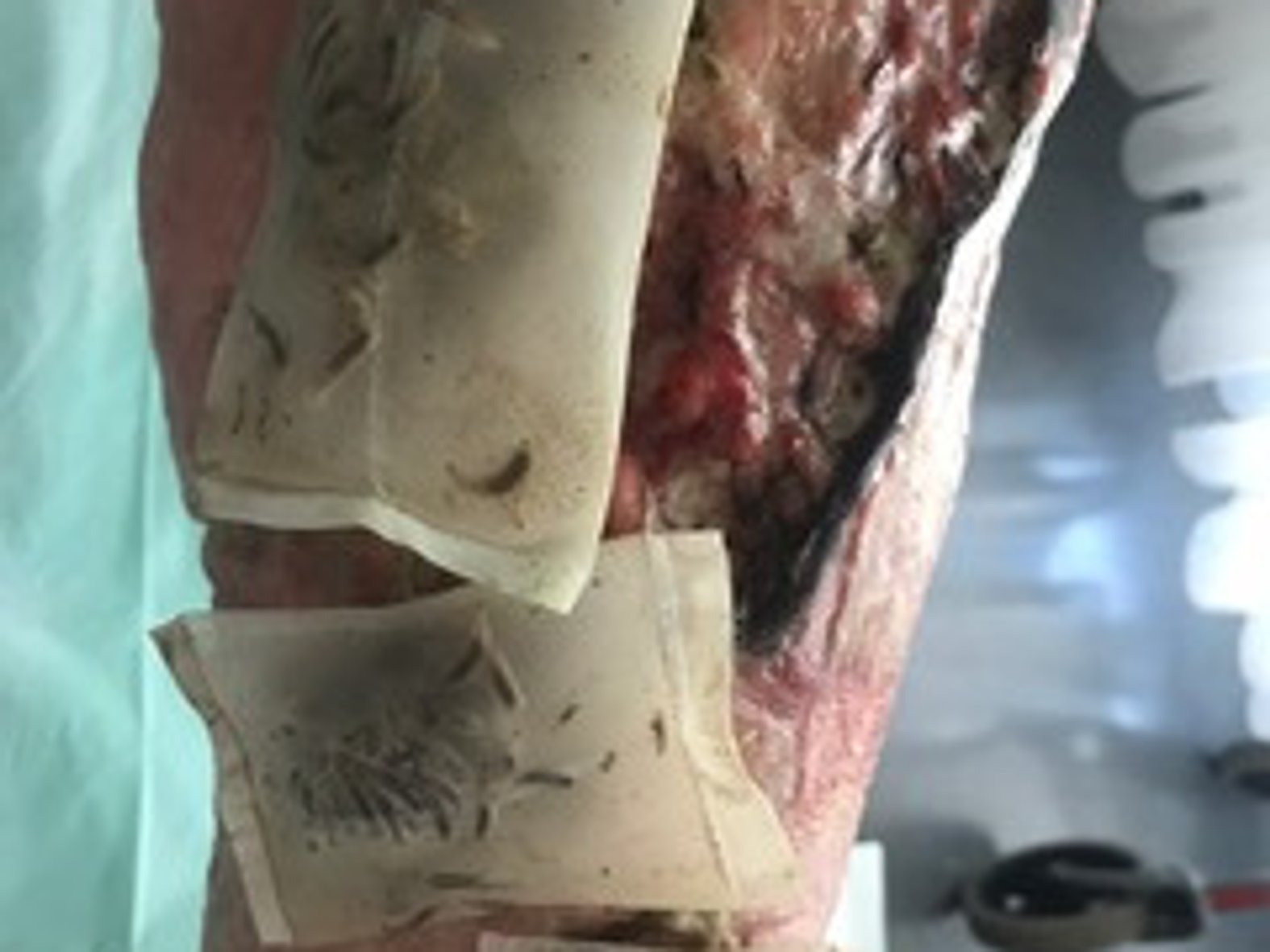
Weil die Larven potentiell Ekel bei Patienten und Pflegepersonal auslösen können und zudem die Gefahr besteht, dass einzelne Larven entkommen, sind die Larven in Deutschland inzwischen hauptsächlich als BioBag® erhältlich. Die Larven werden hierbei in einem Polyesternetz auf die Wunde gesetzt, sodass ein Entwischen „freilaufender“ Larven verhindert wird. Der Vorteil der freilaufenden Larven besteht darin, dass sie jeden Winkel der Wunde erreichen und somit auch z.B. bei zerklüfteten Wunden angewendet werden können.
Vor dem Beginn des Débridements muss die Wunde frei von lokalen Medikamenten wie Antiseptika und Anästhetika sein. Wenn die Wunde im Vorfeld desinfiziert wurde, sollte sie deshalb ordentlich ausgespült werden. Es wird empfohlen, die Larven für eine Anwendungsdauer von bis zu 4 Tagen einzusetzen. Die Wunde sollte für ein optimales Débridement weder zu feucht noch zu trocken sein. Deshalb ist eine tägliche Kontrolle ebenso wie ein täglicher Verbandwechsel wichtig. Dabei kann die Biobag jeweils so repositioniert werden, dass der Wundbelag gleichmäßig abgetragen werden kann. Wenn die Wunde zu stark austrocknet, sollte sie nochmal mit NaCl-Lösung angefeuchtet werden.
Fliegenlarven der Gattung Lucilia sericata
- reinigen die Wunde,
- regen die Exsudatproduktion an,
- vernichten Keime (vor allem grampositive Keime, auch MRSA),
- stimulieren die Wundheilung.
Achtung: Das biochirurgische Débridement sollte nicht zum Einsatz kommen bei:
- zu Blutungen neigenden Wunden
- Wunden mit Nähe zu größeren Gefäßen, Körperhöhlen und/oder inneren Organen
- unzureichend durchbluteten Wunden
- Verabreichung von Antikoagulantien (Gerinnungshemmer)
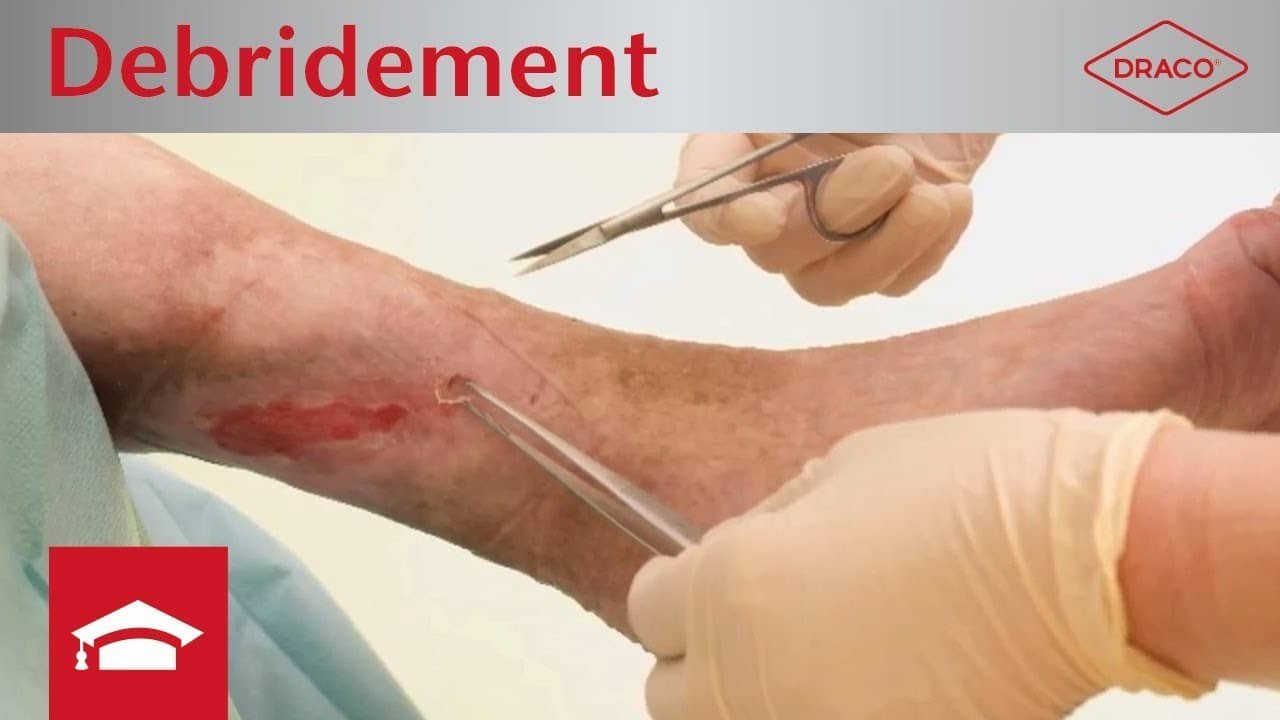
Chirurgisches Débridement
Das chirurgische Débridement ist eine sehr schnelle, jedoch wenig schonende Art des mechanischen Débridements.
Es sollte deshalb nur dann zum Einsatz kommen, wenn schonendere Alternativen nicht möglich sind. Nekrosen und Beläge werden dann z.B. mit Skalpell und Pinzette oder einer Ringkürette von der Wundoberfläche entfernt. Da es sich um ein invasives Verfahren handelt, ist eine genaue Selektion des zu entfernendes Gewebes kaum möglich und Verletzungen umliegender Gewebestrukturen sind nicht immer zu verhindern. Der größte Vorteil des chirurgischen Débridements ist die schnelle, effektive Entfernung von avitalem Gewebe und somit schnelle Senkung der Keimlast, was mithilfe anderer Methoden nur schwer zu erreichen ist.
In Abgrenzung zum chirurgischen Débridement ist oft von einem „scharfen Débridement“ die Rede. Dieses ist als ein kleinerer chirurgischer Eingriff mit Skalpell oder Schere definiert, der (im Unterschied zum chirurgischen Débridement) ohne Teil- oder Vollnarkose auskommt. Während ein chirurgisches Débridement nur von qualifizierten Ärzten durchgeführt werden darf, kann ein scharfes Débridement auch von medizinischem Fachpersonal wie Pflegekräften, Hausärzten oder Dermatologen ohne chirurgische Ausbildung vorgenommen werden.
Durchführung
Je nach Ausmaß und Dicke des zu entfernenden Wundbelags ist eine Kurznarkose oder eine Lokalanästhesie im Vorfeld erforderlich. Wie alle Débridementarten muss auch ein chirurgisches Débridement unter sterilen Bedingungen durchgeführt werden. Die Wunde und die direkte Umgebung werden dafür mit Antiseptika vorbehandelt. Nach dem invasiven Eingriff sollte die Wunde mit einer antiseptischen Lösung gereinigt und je nach Wundgröße und -art mit angemessenen sterilen Wundauflagen versorgt werden.
Da es beim chirurgischen Débridement häufig zu Blutungen kommt, empfiehlt sich z.B. eine zusätzliche Anwendung von Alginaten, da diese leicht blutstillend wirken. In Abhängigkeit des Exsudataufkommens kann eine geeignete Sekundärwundauflage gewählt und falls nötig fixiert werden. Eine Biopsie sollte erfolgen, wenn klinische Zeichen für eine die Wunde gefährdende Kontamination oder Infektion vorliegen.
Achtung: Im Vorfeld eines chirurgischen Débridements sind eventuelle Gerinnungsstörungen und die Einnahme von Gerinnungshemmern mit den Patienten abzuklären.
Enzymatisches Débridement
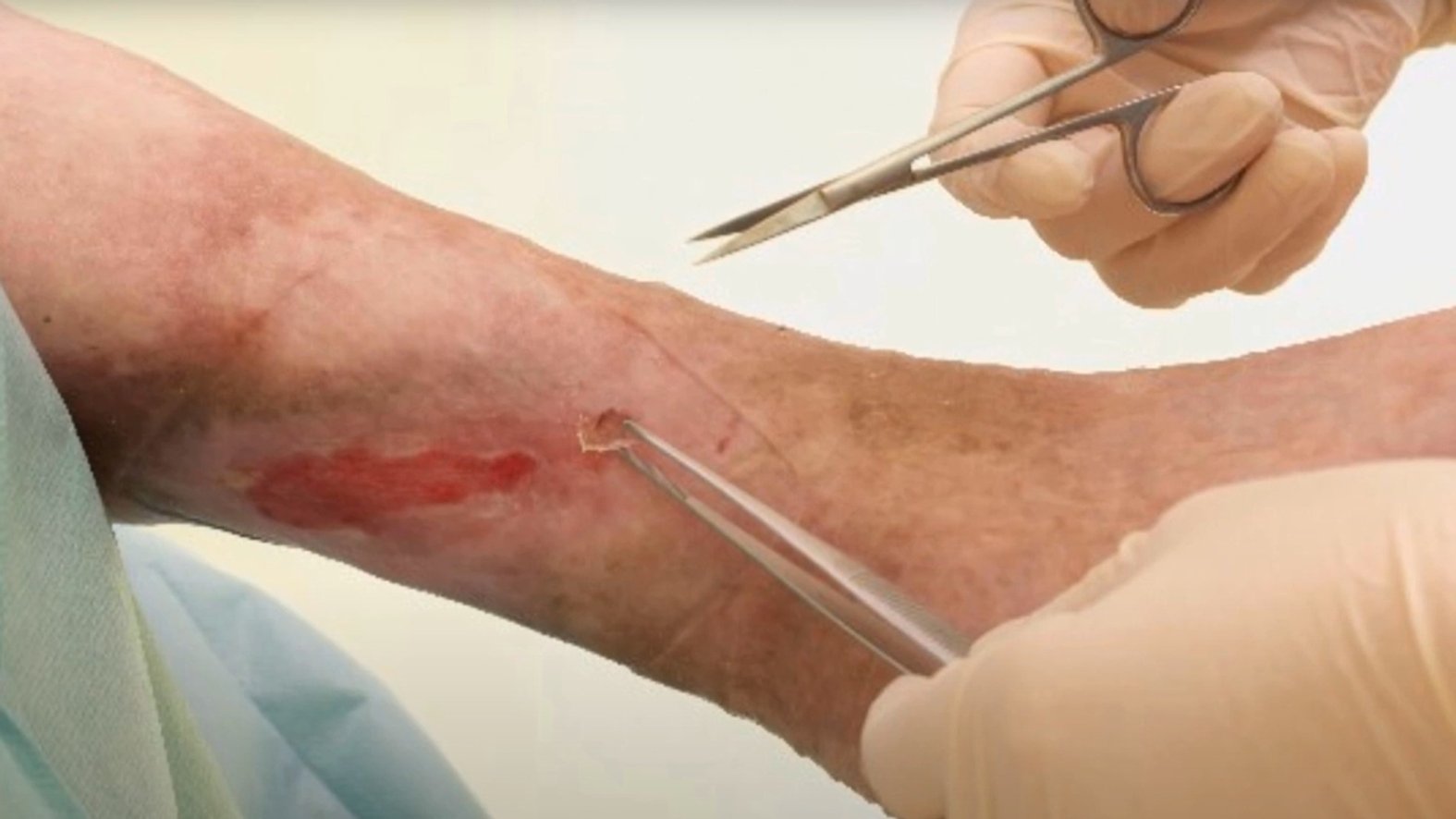
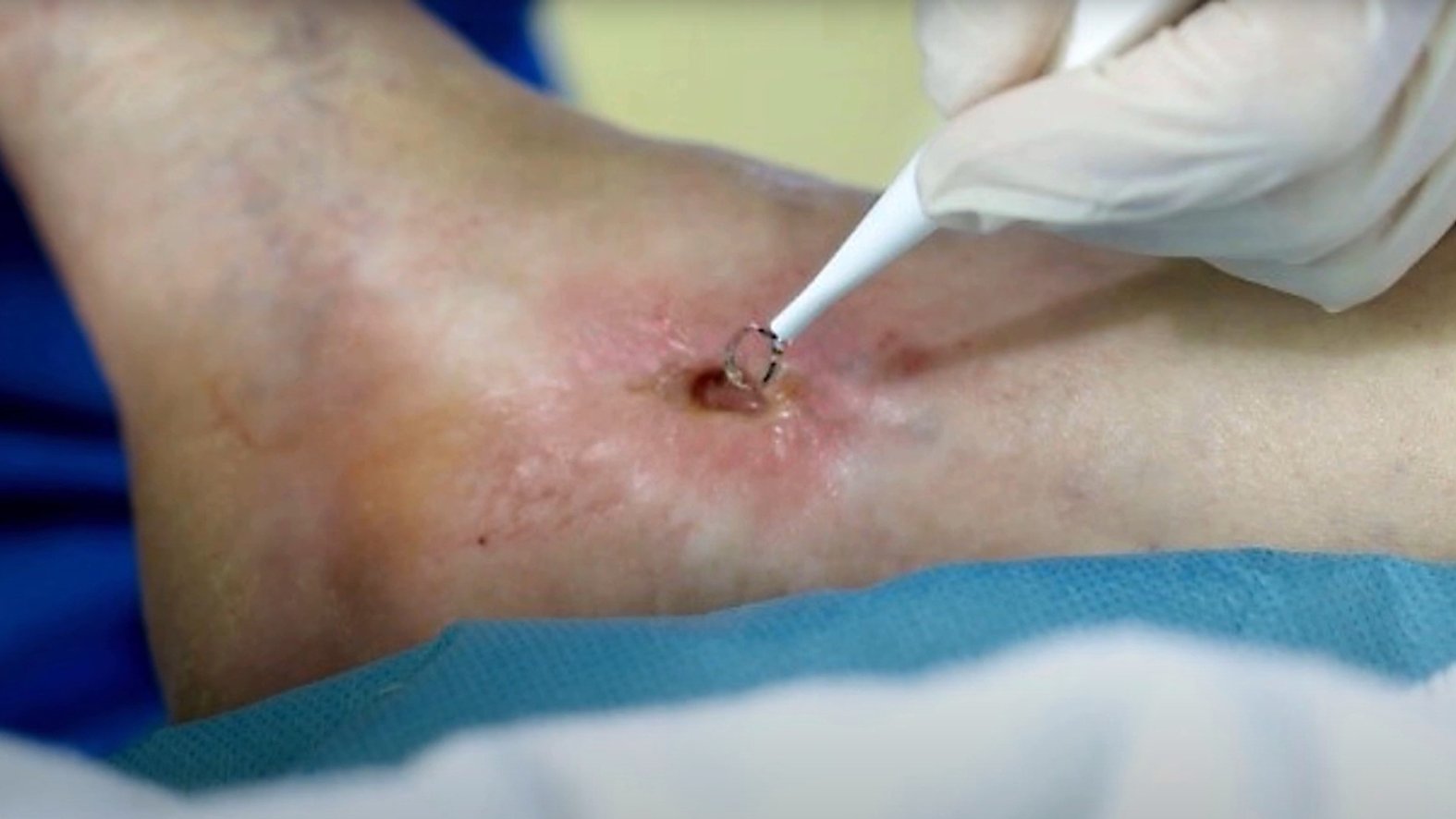
Beim enzymatischen Débridement werden bestimmte proteolytische Enzympräparate als Gele oder Salben aufgetragen, die im Zusammenspiel mit körpereigenen Enzymen Nekrosen und Beläge aufweichen und zersetzen.
Enzymverbände haben eine begrenzte Wirkdauer und sind mindestens einmal am Tag zu wechseln.
Enzymatisches Débridement kommt vor allem dann zum Einsatz, wenn ein mechanisches Débridement nicht möglich ist, zum Beispiel bei Patienten mit Gerinnungsstörungen. Es sollte nur solange, bis die Wunde frei von Gewebetrümmern ist, angewandt werden. Wie beim autolytischen Débridement handelt es sich um eine weitgehend schmerzfreie, aber sehr zeitaufwendige und deswegen unwirtschaftliche Form des Débridements.
Durchführung
Je nach Produkt wird das Präparat ein- bis zweimal täglich 2–3 mm auf den betroffenen Bereich aufgetragen. Darauf kann zunächst ein Wunddistanzgitter wie DracoTüll Silikon aufgelegt werden, um das Verkleben mit der Sekundärwundauflage zu verhindern. Je nach Exsudataufkommen sind sterile Wundauflagen wie DracoPor (bei intakter Wundumgebungshaut), DracoFoam oder DracoSuperabsorber als Sekundärverband möglich, die, falls nötig, fixiert werden müssen.
Achtung: Enzyme benötigen Feuchtigkeit, um ihre Wirkung zu entfalten und sind daher nicht auf trockenen Nekrosen anzuwenden.
Mechanisches Débridement (auch: physikalisches Débridement)
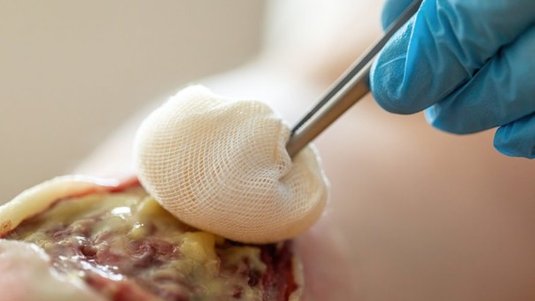
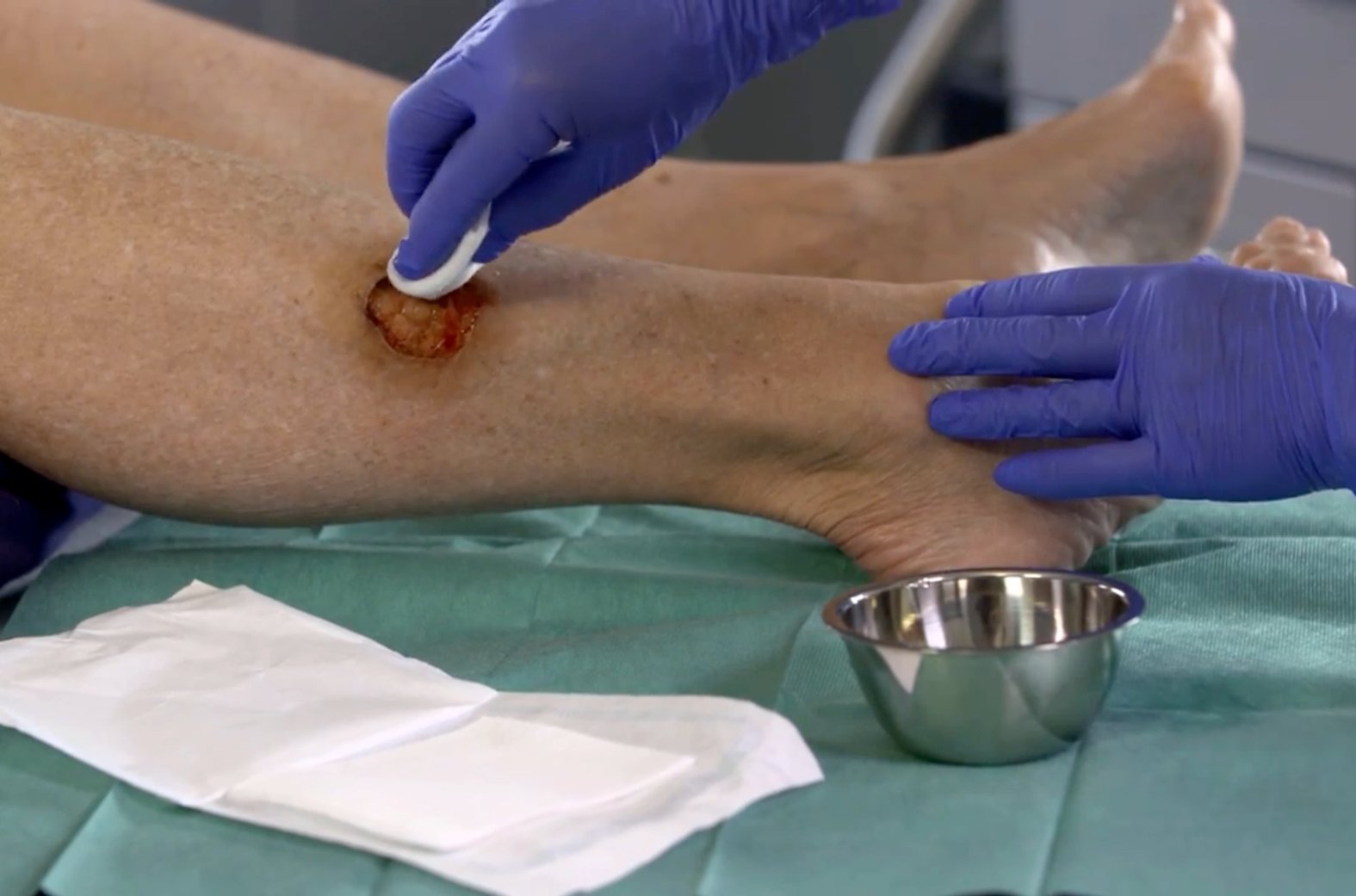
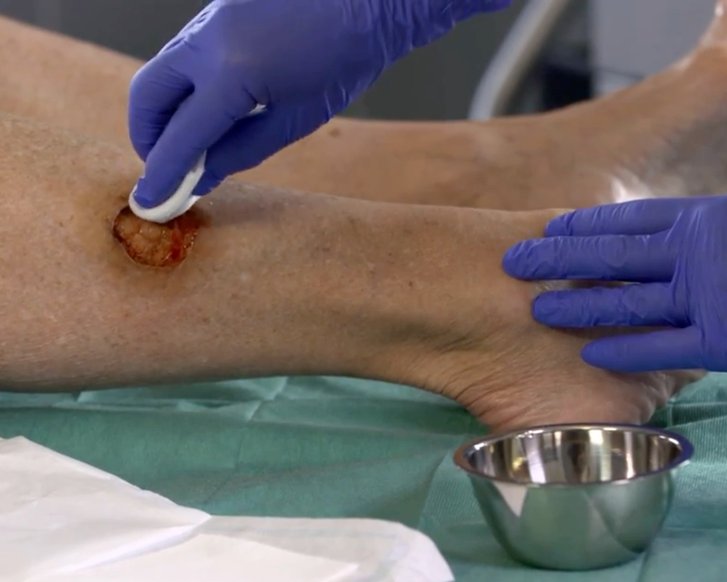
Beim mechanischen Débridement wird die Wunde z.B. mit sterilen Baumwollkompressen und ggf. mithilfe von Pinzetten ausgewischt, um avitales Gewebe bzw. unerwünschte Wundbeläge aus der Wunde zu entfernen.
Es handelt sich um die schnellste und einfachste Art des Débridements, die jedoch für die Patienten teilweise mit Schmerzen verbunden sein kann.
Durchführung
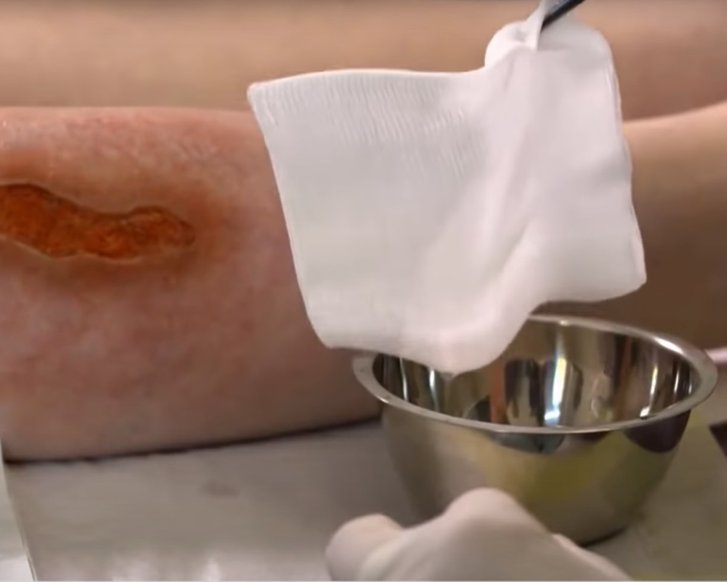
Das mechanische Débridement ist mithilfe unterschiedlicher Methoden und Materialien möglich. Zum Einsatz kommen sterile Kompressen, Monofilamentfaser-Pads, Reinigungstücher und grobporige Schaumstoffe aus Polyurethan. Um Schmerzen zu reduzieren, die durch die Bewegung beim Auswischen der Wunde entstehen können, ist das wiederholte Auflegen angefeuchteter Kompressen mit leichtem Andruck auf die Wunde eine alternative Methode. Der Vorgang kann so oft mit jeweils einer neuen sterilen Kompresse wiederholt werden, bis kein Belag mehr an der Kompresse anhaftet. Wenn ein Teil der Beläge, z.B. festgetrocknete Beläge, so nicht zu entfernen sind, ist die Anwendung der Wet-to-dry-Methode sinnvoll.
Beim Wet-to-dry Débridement wird eine mit steriler Wundspüllösung befeuchtete sterile Kompresse für 10–20 Minuten auf die Wunde bzw. den hartnäckigen Wundbelag aufgelegt. Dabei weicht der Belag auf, verklebt in der Trocknungsphase mit der Gaze und bleibt beim Abnehmen an der Kompresse haften. Je nach Wunde sind mehrere Durchläufe dieses Vorgangs notwendig, von daher ist es mit einem hohen Zeitaufwand verbunden. Es kann zudem zu einer Beschädigung gesunden Gewebes kommen, was Schmerzen bei den Patienten verursachen kann. Die Nutzung von Mikrofaserpads wird von Patienten als schmerzärmer empfunden, allerdings sind diese teurer als Standardkompressen.
Technisches Débridement
Für ein technisches Débridement werden z.B. Ultraschallgeräte, Hydrochirurgie oder Laser eingesetzt.
Hydrochirurgie
Die Hydrochirurgie (auch: Jet-Lavage) ist eine Weiterentwicklung der Wundspülung (Lavage). Bei dieser Methode werden Wundbeläge mithilfe von Flüssigkeiten aus der Wunde gespült. Je nach Verfahren ist dabei auch eine relativ selektive Entfernung von Belägen möglich.
Es kommen verschiedene Verfahren mit unterschiedlicher Intensität zum Einsatz. Als ein sanftes Verfahren ist das einfache Duschen der Wunde zu nennen. Bei intensiveren Verfahren wird die Spülflüssigkeit auf bis zu 1.000 km/h beschleunigt (Hochdruck-Irrigation, Wasserstrahlschneidetechnik, Wasserstrahldissektion). Bei der Wahl der Umgebung ist aufgrund des hohen Applikationsdrucks ein großer Spritzeffekt zu berücksichtigen.
Hydrochirurgische Geräte können relativ flexibel bei vielen verschiedenen Wundarten und Indikationen – von venösen Beingeschwüren bis zur postoperativen Versorgung diabetischer Fußgeschwüre – eingesetzt werden. Die recht teuren Geräte sind in der Regel einfach anzuwenden, bedürfen aber einer regelmäßigen Desinfektion.
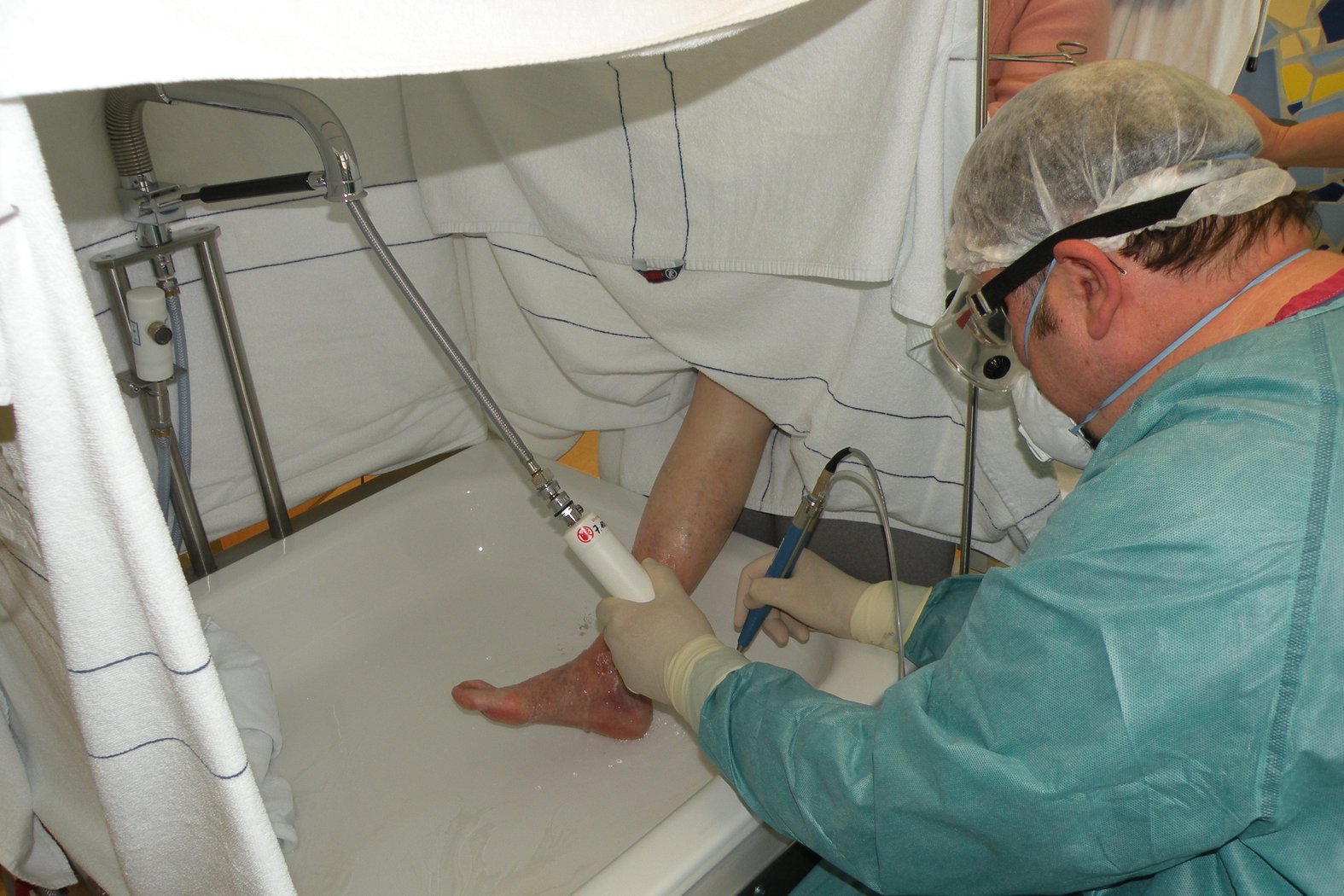
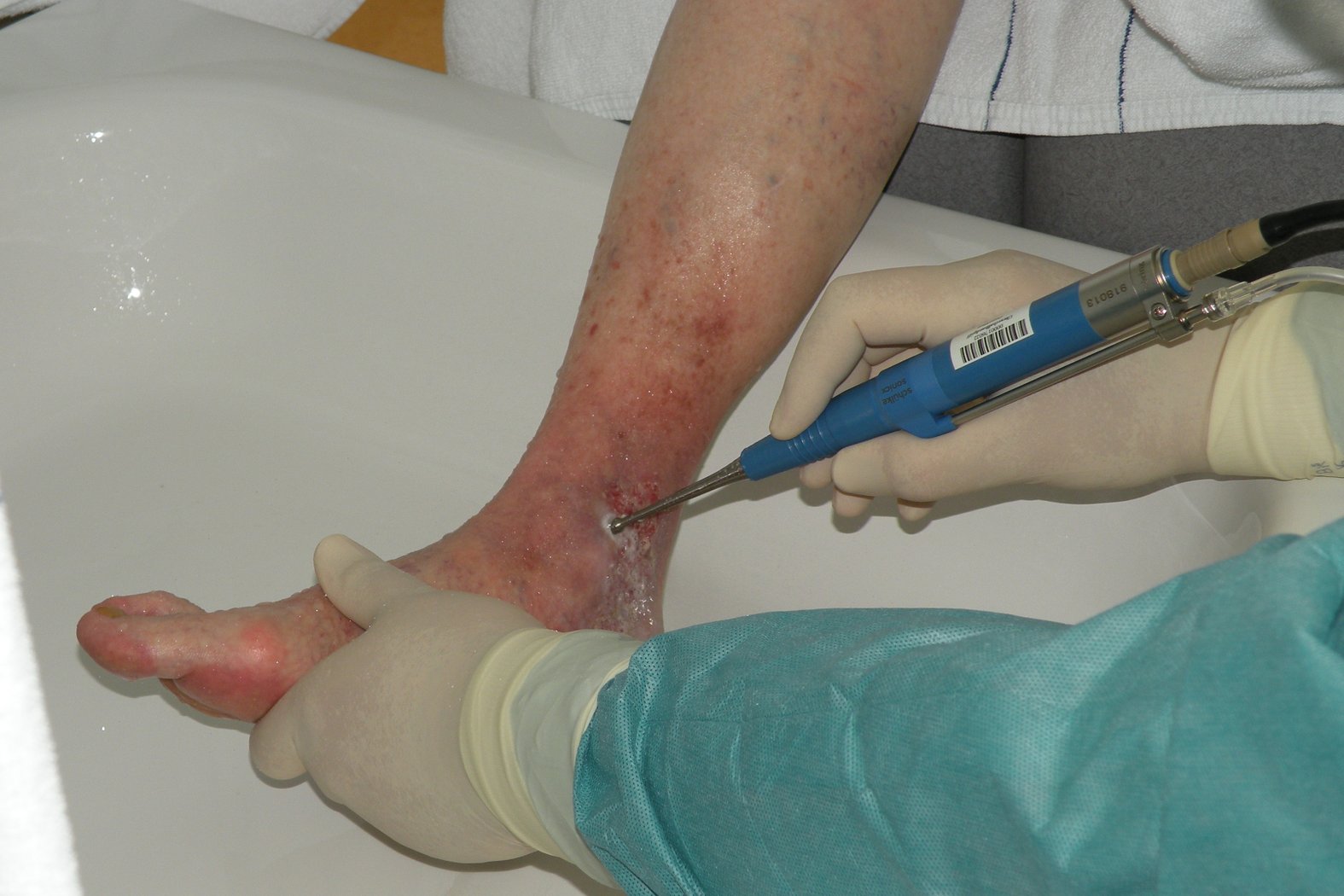
Ultraschall-assistierte Wundreinigung (UAW)
Die UAW nutzt niederfrequenten Leistungs-Ultraschall, der in Kombination mit einer Spüllösung z.B. Fibrinbeläge, Zelltrümmer und Keime aus der Wunde ausspült. Die Spüllösung gelangt durch den Ultraschall-Impuls bis in die tieferen Wundregionen und tötet dort durch Kavitation (zyklisch implodierende Gasbläschen) Bakterien und Pilze ab.
Die ultraschallassistierte Wundreinigung fördert zudem die Granulation, regt die Proliferation der Fibroblasten (Bindegewebszellen) an und stimuliert die Kollagensynthese.
Eine Sonde, aus deren Kopf permanent ein feiner Nebel steriler Spüllösung austritt, wird über die Wunde geführt. Die von der Sonde erzeugten Kavitationseffekte lösen Fibrin, Biofilme und Keime von der Wunde und schonen gesundes Gewebe. Einige Patienten empfinden bei dieser schonenden Débridementart Schmerzen, weshalb sich vorab eine Lokalanästhesie z.B. mit Emla®-Creme empfiehlt.
Achtung: Bei infizierten Wunden sollte eine antiseptische Lösung anstelle einer sterilen Spüllösung verwendet werden.